抗癌活性药物筛选
抗血管肠下形成物质筛选
血管形成在于生长或是发育上扮演重要的角色,用于组织的发育生成和修复。而病理性血管形成存在于许多疾病中包括肿瘤,血管新生会使肿瘤从休眠期转变成恶性、生长迅速、可能侵袭其他组织。越来越多的抗血管形成抑制剂被发现并且进入临床试验,有超过10类用于抗血管形成的药品已经通过过美国食品药品监督管理局的批准。
斑马鱼血管形成模型进行药效学评价和药物新靶点验证获得广泛认可。目前,多支进入临床前实验或者临床试验阶段的抗癌药物(包括已获得FDA批准上市的药物),如Vatalanib (Novartis)、Thalidomide (Celgene)、Compound 6 (TargeGen)、Rosuvastatin、Solenopsin (Eli Lilly)等,均成功地利用斑马鱼血管形成模型进行了有效验证。 在肠下血管发育前给药,可模拟药物对肿瘤部位新生血管的作用。我们可以通过这一原理斑马鱼抗血管形成模型,并用阳性药行了模型的验证,通过在转基因血管绿色荧光斑马鱼品系上评价肠下血管形成抑制率来筛选有效抗血管形成活性物质。
![]()
癌症异种移植模型
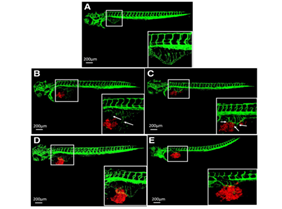
![]()
P糖蛋白Pgp抑制剂筛选
化疗是治疗癌症的重要手段,但化疗中常见且难以解决的问题是肿瘤多药耐药性(Multidrug resistance, MDR)的产生。P-糖蛋白(P-glycoprotein, P-gp)高表达是MDR的形成最主要机制之一,P-gp为跨膜糖蛋白,是肿瘤细胞多药耐药基因MDR1的表达产物,能够与进入细胞浆的抗肿瘤药物结合,将药物从细胞内泵出细胞外,导致肿瘤细胞内药物浓度降低、细胞毒或靶向治疗作用减弱或丧失,进而使肿瘤细胞产生耐药性。因此应用P-gp抑制剂是逆转MDR的一个重要手段。近年来,评价与筛选P-gp抑制剂已成为抗肿瘤药物研究的前沿热点之一。
系统发育学研究证实斑马鱼具有52个ABC转运基因,包括人类所有的48个ABC转运基因,斑马鱼ABC基因与人类ABC基因的同源性高达77%,两者具有一一对应的关系。通过建立了整体斑马鱼P-gp抑制剂筛选模型,通过基于图像或微孔板检测的方法可以快速、高效地进行P-gp抑制剂体内筛选,预测性好、可比度高。
选取特异性荧光染料可以有效的筛选出P-gp抑制剂,因为正常斑马鱼会将此荧光染料泵出体外,而P-gp活性受到抑制的斑马鱼无法正常排出染料后荧光强度增强。我们可以通过这一原理建造斑马鱼P-糖蛋白(P-gp)抑制剂筛选模型,并用阳性药行了模型的验证。
![]()
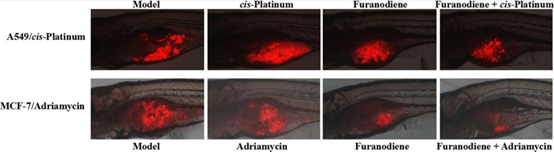
斑马鱼抗肿瘤多药耐药性评价
多药耐药性(MDR)是指肿瘤细胞对一种抗肿瘤药物耐药的同时,对其他结构和作用机制不同的抗肿瘤药物也产生了耐药性。MDR是肿瘤化疗的难点之一,对MDR机制研究及其逆转剂的研究成为研究的热点。MDR的产生机制尚不明确,目前的研究提出几种可能的机制(如细胞膜糖蛋白介导的药物转泄和外排泵机制、酶介导机制等),并根据这些机制,开发钙离子通道阻滞剂、免疫抑制剂、蛋白激酶抑制剂和中药等多药耐药逆转剂,均对逆转肿瘤多药耐药性有不同程度的药效,但开发更安全有效的多药耐药逆转剂,是肿瘤化疗药物开发的方向。
体外抗肿瘤多药耐药性药物筛选实验具有快速高效的优点,但体外实验的药效学与安全性评价结果与人体实验结果的可比性差。体内抗肿瘤多药耐药性药物筛选实验常用的肿瘤移植模型是免疫缺陷的裸鼠,然而这套转移系统存在存活率不确定,需要注射大量细胞、耗时长和维护费用昂贵等问题。因此,开发一种简单、高效、快速和花费低的体内评价模型,对加快抗肿瘤多药耐药性药物开发有着重要意义。
斑马鱼是近年来应用越来越广泛的重要模式生物,作为脊椎动物,与人类基因同源性高达85%,其信号传导通路与人类基本近似,实验结果可比性强,常被用作药物筛选模型。
![]()
靶向抗癌药物筛选Wnt通路
Wnt基因所介导的信号转导通路称为Wnt信号通路,在细胞癌变、肿瘤发生及肿瘤侵袭过程中经常可以看到该通路的异常活化。无论是Wnt基因本身还是通路上任一因素使通路异常活化时,均有可能引起肿瘤的发生。所以阻断异常的Wnt信号通路可以抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡。
我们通过建立了主要基于特异表型的整体斑马鱼筛选模型,可以同时评价靶标抑制或激活、安全性及PK,同时与同一靶标药物或化合物做等浓度相对药效或毒性比较。一旦确定击中靶标,可对相关通路的蛋白和基因进行分析。
在确定候选化合物对Wnt通路确有抑制作用后,可以利用斑马鱼肿瘤异种移植模型和PDX对疗效做进一步评价。


